Ningún producto
Estos precios se entienden sin IVA
Producto añadido correctamente a su compra
Hay 0 elementos en su bolsa de la compra. Hay un elemento en su bolsa d ela compra.
Productos Protección COVID-19
-
Equipos De Protección Individual
- Guantes de Trabajo
- Cascos de Seguridad
- Protección Ocular
- Máscara Soldar
- Pantalla Facial
- Protección Auditiva En El Trabajo
- Protección Respiratoria
- Calzado de Seguridad
- Ropa Técnica Laboral
- Protección Riesgo eléctrico
- Equipos Trabajos Verticales
- Primeros auxilios
- Protección balística
- Protección contra Derrames
- Equipos para Salvamento Marítimo
- Duchas de Emergencia
- Cuchillos de Seguridad
- Detectores de Gases
- Protección Rayos-X
- Protecciones Prevención de Lesiones
- Complementos Epis
- Protección Contra Incendios
-
Vestuario Laboral
- Vestuario Laboral Desechable
- Camisas de Trabajo
- Polos de Trabajo
- Camisetas de Trabajo
- Pantalones de Trabajo
- Monos de Trabajo
- Prendas de Ropa Interior Térmicas
- Forro Polar Trabajo
- Sudaderas de Trabajo
- Jersey de Trabajo
- Cazadoras de Trabajo
- Chaleco de Trabajo
- Chaquetas de Trabajo
- Parka de Trabajo
- Poncho Lluvia Trabajo
- Traje de Lluvia Trabajo
- Chubasqueros de Trabajo
- Ropa de Trabajo Frio Extremo
- Uniformes Hostelería
- Uniformes de Limpieza
- Uniformes Sanitarios
- Uniformes Peluqueria Estética, SPA y
- Frío y lluvia
- Industria Base
- Hostelería y ocio
- Batas de Trabajo
- Equipamiento Sala Blanca
- Complementos
- Calzado de Trabajo
- Señales de Seguridad Señalistica
- Productos Protección COVID-19
- OUTLET EPI
- Equipos de Comunicación
- Medidores
- Cardioprotección
Kit de detección de antígenos del SARS-CoV-2
TestCOVID
Nuevo
Kit de detección de antígenos del SARS-CoV-2
Ensayo inmunocromatográfico con oro coloidal.
Para uso profesional en laboratorios clínicos y profesionales sanitarios que realizan pruebas en su lugar de trabajo.
🚚 Consulte plazos de entrega y política de envíos
- Sacar de mis favoritos
- Agregar este producto a mis favoritos
Kit de detección de antígenos del SARS-CoV-2
Ensayo inmunocromatográfico con oro coloidal.
Para uso profesional en laboratorios clínicos y profesionales sanitarios que realizan pruebas en su lugar de trabajo.
Contenido de la caja:
Material suministrado (25 kits):
- 25 tiras Tira Reactiva de SARS-CoV-2 Ag
- 3 tubos de ensayo de 4 ml de Solución Reactiva de SARS-CoV-2 Ag
- 25 tubos de ensayo
- 25 hisopos orofaríngeos
- Instrucciones de uso
Resumen y descripción:
Los coronavirus son virus ARN de una sola hebra de sentido positivo y no segmentados que pertenecen a la familia de los Coronaviridae y que pueden infectar a personas y a otros mamíferos. Existen algunos casos de infecciones leves por coronavirus en humanos (HCoV-NL63, HCo229E, HCo-OC43 y HKU1), pero los betacoronavirus, que son de origen zoonótico, pueden causar enfermedades graves y mortales como el Síndrome Respiratorio Agudo Severo causado por (SARS-CoV) y el Síndrome Respiratorio de Oriente Medio causado por el coronavirus (MERS-CoV). La pandemia mundial fue causada por el nuevo coronavirus tipo 2 del síndrome respiratorio agudo severo (SARS-CoV-2). El 11 de marzo de 2020 la OMS declaró que el COVID-19 era una pandemia, y que la infección en humanos se había extendido a nivel mundial, con centenares de miles de infectados y muertes confirmadas [1].
Las estimaciones actuales apuntan que el tiempo promedio de incubación es de 5,1 días y se espera que se presenten los síntomas a los 12 días siguientes a la infección [2]. Los síntomas de COVID-19 son similares a los de otras enfermedades respiratorias virales: fiebre, tos y dificultad respiratoria [3].
Uso previsto:
Este kit de detección in vitro se utiliza para la determinación cualitativa de los antígenos del SARS-CoV-2 (proteína N y proteína S) en muestra de hisopo nasal, muestra de hisopo nasofaríngeo o muestra de hisopo orofaríngeo. El antígeno es generalmente detectable en las muestras de las vías respiratorias superiores durante la fase aguda de la infección.
Los resultados positivos indican la presencia de antígenos virales, pero se necesita una evaluación clínica del historial del paciente e información de diagnóstico para determinar el estado de la infección. Los resultados positivos no descartan una infección bacteriana ni infecciones concomitantes con otros virus. Es posible que el agente detectado no sea la causa definitiva de la enfermedad.
Los resultados negativos en pacientes sintomáticos de más de cinco días, deben tratarse como casos sospechosos, pudiéndose realizar una confirmación con un ensayo molecular (PCR), si es requerido en el paciente. Resultados negativos no descartan la presencia de COVID-19 y no deben utilizarse como única base para determinar decisiones sobre tratamiento de pacientes o control de infección. Resultados negativos deben considerarse en el contexto de las exposiciones recientes del paciente, su historial y la presencia de signos y síntomas clínicos coherentes con COVID-19.
Principio del procedimiento:
Se utiliza una técnica de inmunocromatografía de membrana que usa anticuerpos.
La tira reactiva del dispositivo se compone de:
- Una almohadilla que contiene el conjugado de oro coloidal acoplado con anticuerpos específicos del SARS-CoV-2,
- Una membrana de reacción de nitrocelulosa que contiene una línea de prueba (línea T) y una línea de control (línea C). La línea T está recubierta con anticuerpos específicos del SARS-CoV-2, y la línea C está recubierta con anticuerpos anti-ratón en cabras. Cuando los antígenos del SARS-CoV-2 están presentes en la muestra, la banda línea T se volverá roja. Si los antígenos del SARS-CoV-2 no están presentes o están presentes por debajo del umbral de sensibilidad, no se producirá color en línea T. Independientemente de la presencia de antígenos del SARS-CoV-2, la banda de la línea de control (C) siempre debe aparecer en rojo. La línea C sirve como control cualitativo interno del sistema de prueba para indicar que se ha aplicado un volumen adecuado de la muestra y se ha producido el flujo.
Condición de almacenamiento y fecha de caducidad:
Almacene todos los reactivos a 2 °C - 30 °C durante 12 meses. La tira reactiva está protegida por un envoltorio de papel de aluminio. Se recomienda usarla sin exceder los 20 minutos después de desenvolverla. La fecha de caducidad del kit está marcada en el envoltorio con la etiqueta de caducidad de cada uno de los componentes.
Recolección de muestras.
Muestra de hisopo orofaríngeo (proporcionado en el kit): Utilice un hisopo orofaríngeo, inserte el hisopo en las zonas posteriores de la faringe y las amígdalas. Frote el hisopo sobre ambos pilares amigdalinos y la orofaringe posterior sin tocar la lengua, los dientes y las encías.
Transporte y almacenamiento de muestras:
Las muestras deben ser analizadas tan pronto como sea posible después de su recolección. Según los datos generados con la detección del antígeno SARS-CoV-2, los hisopos nasales o nasofaríngeos son estables hasta 48 horas a temperatura ambiente de 2°C a 8°C.
Procedimiento de la prueba:
- Es obligatorio leer las instrucciones antes de usar este kit. Los componentes del kit y las muestras deben alcanzar la temperatura ambiente (entre 18°C a 25°C) al menos 20 minutos antes de la prueba.
- Escriba el número de identificación de la muestra que se va a analizar en el área de identificación de la tarjeta de prueba.
- Ponga 10 gotas (300μl -400μl) de la Solución Reactiva en el Tubo de Ensayo Reactivo.
- Coloque la muestra del hisopo del paciente en el Tubo de Ensayo Reactivo.
- Gire el hisopo al menos 3 veces mientras presiona la cabeza del hisopo contra el fondo y el lateral del tubo de ensayo.
- Deje el hisopo en el tubo de ensayo durante 1 minuto.
- Apriete la cabeza del hisopo contra las paredes del tubo de ensayo mientras lo retira.
- Posteriormente, deseche el hisopo a los residuos de riesgo biológico.
- Pipetee 3 gotas (100μl -120μl) de la muestra del paciente del tubo de ensayo, en la cavidad para la muestra identificada como (S).
- Después de la carga, la tira reactiva debe dejarse a temperatura ambiente y el resultado puede leerse a los 3 minutos y nunca después de haber pasado 20 minutos.
- Examine el resultado antes de 20 minutos.
- El resultado no es válido después de 20 minutos.
Resultados previstos:
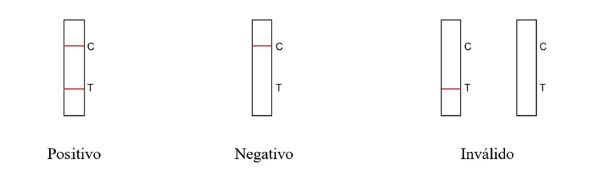
Para la interpretación de los resultados, consulte las gráficas más abajo.
Positivo: Si aparecen tanto la línea C como la línea T, en la ventana de resultados, indica que se han detectado los antígenos del SARS-CoV-2 y el resultado es positivo.
Negativo: Si sólo aparece la línea C en la región de control, la prueba indica que no se detectan antígenos del SARS-CoV-2 y el resultado es negativo.
No válido: Cuando no aparezca ninguna línea de control C antes de 20 minutos, repita la prueba con un nuevo dispositivo de kit, este resultado se considera inválido.
Aviso: La línea de prueba T puede ser de un color mucho más clara que la línea de control C, este resultado será considerado como positivo siempre que la línea roja sea visible.
Control de calidad:
En la prueba se incluye un control de procedimiento. La línea C debe aparecer siempre con una banda roja, se considera un control de procedimiento interno. Esto constata un volumen de muestra suficiente, una tira reactiva y una técnica de procedimiento correctas.
Limitaciones de la prueba:
- Esta prueba de ensayo cualitativo diagnóstico in vitro se limita a profesionales sanitarios. Los resultados positivos de las pruebas no descartan las coinfecciones con otros patógenos. Los resultados positivos de las pruebas no diferencian entre el SARS-CoV y el SARS-CoV-2. Los resultados negativos de las pruebas no están destinados a descartar otras infecciones virales o bacterianas que no sean SARS. Los resultados negativos de pacientes sintomáticos de más de cinco días, deben tratarse como casos sospechosos y se puede realizar una confirmación con un ensayo molecular (PCR), si es requerido en el paciente.
- El kit de detección está diseñado solamente como diagnóstico in vitro y para la detección de antígenos del SARS-CoV-2 (proteína N y proteína S) en una muestra de recolección de los hisopos indicados en estas instrucciones de uso. El resultado es sólo un análisis cualitativo, no una detección cuantitativa.
- Examine el resultado antes de 20 minutos. El resultado no se considera válido después de los 20 minutos.
Comentarios
No hay comentarios de clientes por ahora.
Summary
- Product Name:Kit de detección de antígenos del SARS-CoV-2
- Product Reference: TestCOVID
- Price: 225,00 €
- Product Width: 0.00 cm
- Product Height: 0.00 cm
- Product Depth: 0.00 cm
- Product Weight: 0.00 kg
- Description: Kit de detección de antígenos del SARS-CoV-2 Ensayo inmunocromatográfico con oro coloidal. Para uso profesional en laboratorios clínicos y profesionales sanitarios que realizan pruebas en su lugar de trabajo.